新聞詳情
出乎意料的癌癥**療法與疼痛的關(guān)聯(lián)
日期:2024-08-29 09:37
瀏覽次數(shù):558
摘要:
出乎意料的癌癥**療法與疼痛的關(guān)聯(lián)
癌癥**療法被譽(yù)為癌癥**中的里程碑突破,但是越來(lái)越多的醫(yī)師們注意到此類(lèi)療法引發(fā)了新的副作用,如嚴(yán)重過(guò)敏反應(yīng),急性發(fā)作的糖尿病和心臟損傷。一些通過(guò)釋放**系統(tǒng)來(lái)抵**癥的**僅僅在約五分之一的病例中有效,這令許多患者開(kāi)始懷疑這一療法的可靠性。
不過(guò)*新一項(xiàng)研究指出,可以通過(guò)一種快速簡(jiǎn)單的方法來(lái)預(yù)測(cè)哪些癌癥患者可能可以從**療法中受益,從而進(jìn)行個(gè)體化**。
研究人員發(fā)現(xiàn)目前流行的**療法**nivolumab阻斷的分子:PD...
出乎意料的癌癥**療法與疼痛的關(guān)聯(lián)
癌癥**療法被譽(yù)為癌癥**中的里程碑突破,但是越來(lái)越多的醫(yī)師們注意到此類(lèi)療法引發(fā)了新的副作用,如嚴(yán)重過(guò)敏反應(yīng),急性發(fā)作的糖尿病和心臟損傷。一些通過(guò)釋放**系統(tǒng)來(lái)抵**癥的**僅僅在約五分之一的病例中有效,這令許多患者開(kāi)始懷疑這一療法的可靠性。
不過(guò)*新一項(xiàng)研究指出,可以通過(guò)一種快速簡(jiǎn)單的方法來(lái)預(yù)測(cè)哪些癌癥患者可能可以從**療法中受益,從而進(jìn)行個(gè)體化**。
研究人員發(fā)現(xiàn)目前流行的**療法**nivolumab阻斷的分子:PD-L1不僅能影響**細(xì)胞,而且也能作用于產(chǎn)生疼痛的神經(jīng)細(xì)胞。這將可作為一種簡(jiǎn)單的檢測(cè),分析疼痛敏感性的微妙差異,從而衡量身體是否會(huì)對(duì)**作出反應(yīng)。
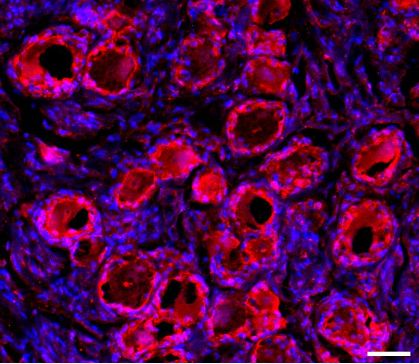
人背根神經(jīng)節(jié)DRG上的感覺(jué)神經(jīng)元會(huì)由于PD-1顯示紅色,藍(lán)色顯示為細(xì)胞核。
這一研究成果公布在5月22日的Nature Neuroscience雜志上,揭示了癌癥的“秘籍”——它會(huì)利用各種技巧來(lái)逃避身體自然防御機(jī)制的篩查。
領(lǐng)導(dǎo)這一研究的是杜克大學(xué)醫(yī)學(xué)中心神經(jīng)生物學(xué)系教授,教育部長(zhǎng)江學(xué)者獎(jiǎng)勵(lì)計(jì)劃講座教授和復(fù)旦大學(xué)講座教授紀(jì)如榮教授,紀(jì)如榮教授是近年來(lái)國(guó)際慢性痛研究領(lǐng)域的重要領(lǐng)軍人物之一,他的研究工作在國(guó)際上得到廣泛認(rèn)可,近年來(lái)發(fā)表高質(zhì)量的SCI學(xué)術(shù)論文一百余篇。文章的另外一位通訊作者是復(fù)旦大學(xué)特聘教授張玉秋教授。

對(duì)于這項(xiàng)*新成果,紀(jì)教授表示,“癌細(xì)胞十分聰明,之前已經(jīng)發(fā)現(xiàn)它們能生成PD-L1抑制**系統(tǒng)。但它們還有另外一個(gè)防守系統(tǒng),那就是疼痛,我們的這項(xiàng)研究表明這個(gè)知名的分子可以掩蓋疼痛,所以癌癥可以在轉(zhuǎn)移前,不發(fā)出任何報(bào)警的情況下進(jìn)行生長(zhǎng)?!?
在癌癥發(fā)生的早期階段,當(dāng)癌細(xì)胞剛剛開(kāi)始在某些組織和器官中生長(zhǎng)時(shí),這種**并不會(huì)帶來(lái)疼痛,但是隨著癌癥越來(lái)越侵襲,遍布到了全身,這些細(xì)胞就會(huì)分泌許多誘導(dǎo)疼痛的化學(xué)物質(zhì),引發(fā)神經(jīng)纖維痛覺(jué)感知,或者生成神經(jīng)生長(zhǎng)因子之類(lèi)的分子,構(gòu)建新的神經(jīng)纖維。這種疼痛有可能變得無(wú)法忍受,因?yàn)橐恍┗颊呔褪撬烙?*樣**過(guò)量。
紀(jì)教授已經(jīng)從事了二十多年的疼痛學(xué)研究,*近其研究小組發(fā)現(xiàn)患有黑色素瘤的小鼠模型并沒(méi)有出現(xiàn)其它癌癥類(lèi)型小鼠中的疼痛跡象,后者如果出現(xiàn)不舒服就會(huì)縮回或舔它們的后爪。
黑素瘤細(xì)胞能產(chǎn)生一種稱(chēng)為PD-L1的分子,這種分子結(jié)合在白細(xì)胞表面PD-1受體上,能有效的遏制**應(yīng)答。紀(jì)教授希望了解這其中是否存在關(guān)聯(lián),為此他們利用nivolumab**小鼠,這是一種能阻止PD-L1與PD-1結(jié)合的**。然后,研究人員又用測(cè)量細(xì)絲戳小鼠的后爪,檢測(cè)它們收回后爪所需的力量。結(jié)果發(fā)現(xiàn)令小鼠縮回后爪所需的力要比**前要小得多,這表明它們對(duì)疼痛變得更加敏感。此外,他們還發(fā)現(xiàn)nivolumab會(huì)引起黑色素瘤小鼠的自發(fā)性疼痛。
接下來(lái),研究人員進(jìn)行了反向?qū)嶒?yàn):他們將PD-L1(疼痛掩蓋因子)注射到了三種不同疼痛類(lèi)型(炎性疼痛,神經(jīng)性探討和骨癌疼痛)的小鼠模型中,結(jié)果表明在每種情況下,注入PD-L1都具有鎮(zhèn)痛作用,能令小鼠對(duì)疼痛的敏感性降低。
“這種作用效果驚人的快,我們?cè)诎胄r(shí)內(nèi)就看到疼痛減輕的狀況,”紀(jì)教授說(shuō)。
為了弄清楚這一快速反應(yīng)的機(jī)制,研究人員又分析了背根神經(jīng)節(jié)(DRG)中的感覺(jué)神經(jīng)元,這一神經(jīng)節(jié)是脊髓頂部附近神經(jīng)和神經(jīng)元的集合。他們從小鼠DRGs以及來(lái)自捐贈(zèng)者的人DRGs中分離得到了這些細(xì)胞,并將其培養(yǎng)在含有或不含有PD-L1的培養(yǎng)皿中,記錄它們的電活性。研究人員發(fā)現(xiàn)PD-L1能損壞鈉離子通道啟動(dòng)神經(jīng)元(動(dòng)作電位)對(duì)疼痛感知的能力。
這一發(fā)現(xiàn)不僅能促進(jìn)新疼痛**方法的研發(fā),而且還能預(yù)測(cè)基于PD-1和PD-L1現(xiàn)有**的療效,“對(duì)癌癥**的反應(yīng)可能需要很長(zhǎng)時(shí)間,幾周到幾個(gè)月,而疼痛的反應(yīng)在幾分鐘到幾個(gè)小時(shí)能就會(huì)發(fā)生。”
未來(lái),紀(jì)教授希望能分析這一機(jī)制是否也適用于其它****,同時(shí)他也將與臨床醫(yī)生一起檢測(cè)患者**后疼痛敏感性的變化,這也是進(jìn)行診斷檢測(cè)的**步。




